*Решетов И.В., *Стрельцова Е.А., Головаченко В.А.
*ФГУ МНИОИ им. П.А.Герцена, отделение микрохирургии (г. Москва)
Актуальность проблемы
История хирургии полых и трубчатых органов напрямую связана с поиском эффективного способа герметизации швов с целью предупреждения развития опасных для жизни осложнений. В связи с этим в ведущих хирургических клиниках ведутся активные поиски дополнительных методов герметизации анастомозов.
В течение многих лет большие надежды были связаны с возможностью герметизации швов с помощью биологических или синтетических клеевых композиций. С 70-х годов прошлого века в хирургических стационарах начали применять в качестве вспомогательного метода биоинертные многокомпонентные фибриновые клеи. Производство таких клеев связано с достаточно сложными технологиями, а широкое их применение в клинике ограничивается неуверенностью в прочности и достаточной адгезивности полимеризованной плёнки и чрезвычайно высокой стоимостью. В середине прошлого века были синтезированы цианокрилатные клеи (ЦК), которые постоянно совершенствуются и применяются в хирургии полых и паренхиматозных органов. Однако, в процессе клинического использования был выявлен ряд недостатков (гидрофобность и необходимость перед апликацией предварительного высушивания тканей, общая и местная гистотоксичность, высокая скорость отверждения плёнки и возможность её отторжения в ранний срок после операции, длительные (до 1,5 лет) сроки биодеградации, сложность технологии изготовления, что определяет высокую экономическую стоимость ЦК), не позволяющих широко использовать данный продукт в клинической практике.
После предварительного отбора (плацебо) и сравнительной оценки эффекта аппликации на ткани экспериментальных животных из нескольких препаратов (таблица 1), производных латекса, был выявлен нитрилакриловый латекс, отличающийся умеренной вязкостью и текучестью, гидрофильностью и высокой адгезивностью, а также визуально наблюдаемым внедрением в подкожную клетчатку и адвентизацию артерий и вен с образованием в течение 3-4 минут на поверхности тканей тонкой прозрачной пленки. При гистологической оценке воздействия латекса отмечены минимальные изменения в исследованных тканях (Таблица 2). По химическому составу нитрилакриловый латекс представляет собой коллоидную водную дисперсию полимеров, ограниченно набухающих в воде. Полимерная его часть не содержит двойных связей и токсичных радикалов в отличие от ЦК. Для придания композиции антисептических, бактерицидных и противовоспалительных свойств в её состав был включен диоксидин и Е-аминокапроновая кислота. Учитывая заявленные характеристики клея производителем, нами на этапе сертификации была проведена клиническая апробация данного продукта в клинике опухолей головы и шеи и реконструктивно-пластической хирургии. Основным критерием эффективности являлось статистически достоверные показатели снижения числа послеоперационных осложнений; критерием безопасности послужило число побочных явлений, обусловленных применением ЛТК.
Материалы и методы
Используемый клей представляет из себя стерильную пластиковую ампулу объемом 1 мл. Каждая из ампул имеет отдельную стерильную упаковку в виде запаянного полимерно-бумажного пакета.
Во всех случаях ЛТК наносился на линии швов сформированных анастомозов. Методика наложения клея состояла из вскрытия контейнера с композицией и нанесения клеевой композиции на линию швов анастомоза. При этом ЛТК наносился не только на линию анастомоза, но и на 15–20 мм проксимальнее и дистальнее её, образуя тонкую эластичную пленку. Полная полимеризация клеевой композиции происходила при комнатной температуре от 5 до 10 минут, в зависимости от толщины образовавшейся плёнки.
В нашей клинике ЛТК использовался для различных видов герметизации, учитывая то, что при выполнении онкологических и реконструктивно-пластических операций использовались разнообразные по тканевым свойствам трансплантаты.
Результаты применения клея в клинике
Клеевые композиции в виде тканевого латексного клея (ЛТК) были применены более чем у 30 пациентов, с различной опухолевой патологией (см. таблицу 3).
Основную группу составили пациенты с наиболее распространённой патологией гортани и гортаноглотки. При выполнении операции на полости рта и гортаноглотке с целью герметизации шва на полом органе клей наносился на механическую или ручную линию швов перед закрытием раны. Далее рана послойно ушивалась с оставлением дренажей (см. рисунок 1).
Вторую большую группу составили пациенты с дефектами ТМО, образующихся после нейрохирургических операций. Эта очень интересная группа больных, так как дефекты ТМО мы восстанавливали различными способами (сшивание ТМО при небольших линейных дефектах, использование перемещенного надкостничного лоскута, использование микрохирургического сальникового аутотрансплантата). Во всех случаях мы дополнительно герметизировали ТМО при помощи ЛТК (рисунок 2).
У небольшой группы пациентов клей применялся в качестве дополнительной герметизации сосудистого шва с использованием алло- и аутотрансплантатов (рисунок 3). Учитывая высокое давление в магистральных сосудах, дополнительная обработка клеем представляется интересной находкой, позволяющая снизить процент несостоятельности анастомозов.
Также клей использовался для дополнительной герметизации костных дефектов, образующихся при заборе микрохирургических лоскутов для реконструкции. Помимо традиционных гранул гидроксиапатита (ГАП) на дефекта кости был нанесён клей. Отмечено хорошее заживление донорской раны в послеоперационном периоде, укорочение сроков реабилитации. Сочетание ЛТК с ГАП использовалось при различных костных дефектах (нижняя челюсть, малоберцовая кость, гребень подвздошной кости, лучевая кость и др.). Во всех клинических случаях отмечалось отсутствие тканевой реакции, быстрое формирование костной мозоли, неплохие функциональные результаты. При рентгенологическом контроле отмечалось полное заполнение дефекта клеем латексным тканевым с гранулами гидроксиапатита.
При использовании клея для герметизации кожных швов в случаях с высоким риском несостоятельности (высокое натяжение тканей вследствие значительного дефекта, анатомические зоны с повышенным риском расхождения швов) на поверхности формировалась тонкая защитная плёнка. В одном наблюдении отмечалась местная гиперемия кожи вдоль длинника швов, возможно связанная с индивидуальной реакцией гиперчувствительности пациента. Перспективным нам показалось использование клея при обработке швов на оро-, трахеостоме, так как указанные анатомические области подвергаются воздействию агрессивной среды (слюна), что часто является пусковым фактором при развитии несостоятельности.
Обсуждение полученных результатов
Одним из самых частых оперативных вмешательств в отделениях опухолей головы и шеи, выполняемых по поводу рака гортани, является ларингоэктомия. Стоит отметить, что большая часть пациентов проходила дистанционную лучевую терапию (ДЛТ) в предоперационной (40-45 Гр.) или полной дозах лучевой терапии (65-75 Гр.). Первичное заживление раны у данной группы затруднительно, что обусловлено снижением эластичности облученных тканей, и, как следствие, крайне низкой способности таких тканей к нормальной регенерации. Основной проблемой у таких больных в послеоперационном периоде является формирование глоточного свища, что значительно удлиняет сроки нахождения больного в стационаре, во-первых, а, во-вторых, отодвигает сроки восстановления питания пациента через рот.Данные, приведённые в таблице 4, демонстрируют частный пример использования продукта в онкологической клинике. Нами была отобрана группа пациентов для анализа после ларингоэктомии как одной из наиболее распространённых нозологий при опухолях головы и шеи. Для объективизации результатов была использована контрольная группа пациентов. За период сентябрь 2006 – март 2007 года в отделении микрохирургии МНИОИ было выполнено около 25 ларингоэктомий с одномоментным ушиванием гортаноглотки (см. таблицу 4). Были сформированы 2 группы: половине пациентов линия швов на гортаноглотке обрабатывалась клеем: из них у 17 пациентов была предоперационная или полная доза ЛТ, у одного пациента курс ПХТ. Учитывая опыт отделения в проведении подобных операций, процент осложнений не высок, глоточные свищи возникли у 3-х пациентов из контрольной группы.
При герметизации дефектов ТМО использовались различные варианты закрытия дефектов. Части пациентов клей был нанесен непосредственно на ТМО перед закрытием дефекта надкостничным лоскутом. После получения первых положительных результатов, мы использовали ЛТК в более сложных вариантах реконструктивных вмешательств. При обширных опухолях, инфильтрирующих ТМО на значительном протяжении, требуется пластическое закрытие с использованием широкой фасции бедра, микрохирургического сальникового лоскута и др. Для дополнительной прочности использовалась полипропиленовая сетка. Во всех случаях клеем дополнительно обрабатывались места соединения различных тканей. При оценке послеоперационного периода у данной группы пациентов отмечена надёжная герметизация, благодаря которой послеоперационное осложнение в виде ликворреи сведено к минимуму. При сравнении с традиционным герметиком – фибрин-тромбиновым клеем – при использовании ЛТК отмечена достаточная клиническая эффективность.
Выводы
Накопленный нами опыт по использованию клея латексного тканевого, позволяет рекомендовать данный продукт к использованию в клинике. На примере клинической группы пациентов, представленной в таблице 3, показано, что ЛТК успешно применяется на разнородной группе тканей. Помимо ожидаемого эффекта действия на слизистой оболочке полых органов, ЛТК оказался эффективным и ареагенным на соединительных тканях (ТМО, оболочки сосудов, костная ткань). Помимо отличных адгезивных свойств, клей обладает гемостатическим эффектом при применении его на слизистой оболочке. При применении у стомированных пациентов в качестве изоляции от попадания слюны отмечено гладкое течение послеоперационного периода.
Минимальное количество осложнений, полученных при использовании клея, дополнительно подтверждают его клиническую безопасность.
Стоит отметить удобство применения (отсутствие сложностей при нанесении клея в труднодоступные участки (рисунок 4), хорошие функциональные результаты, статистически достоверное снижение общего числа послеоперационных осложнений позволяет рекомендовать продукт для использования в клинике реконструктивной хирургии у онкологических больных.
Приложение
Таблица 1. Сравнительный морфологический анализ при применении ЦК и ЛТК
Гистологические изменения в коже и подкожной клетчатке на 3 сутки после аппликации цианкрилатного клея
|
Гистологические изменения в коже и подкожной клетчатке на 3 сутки после аппликации ЛТК
|
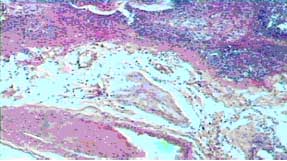 |
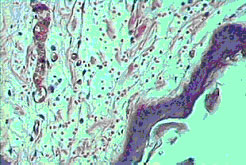 |
Таблица 2. Влияние аппликации ЛТК на гистологические изменения в слизистой оболочке тонкой кишки
Проксимальный отдел тонкой кишки, 7 сутки после аппликации ЛТК. Окраска гематоксилин-эозином Х 600.
|
Дистальный отдел тонкой кишки, 7 сутки после аппликации ЛТК. Окраска гематоксилин-эозином Х 600.
|
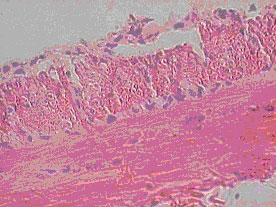 |
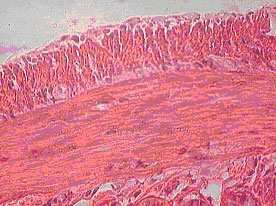 |
Таблица 3. Общая характеристика групп пациентов
Тип герметизации
|
Общее количество пациентов
|
Осложнения
|
Шов на глотке
|
13
|
1 (слюнной свищ)
|
Пластика дефектов ТМО
|
8
|
1 (ликворрея)
|
Пластика дефекта сосуда
|
2
|
0
|
Пластика костных дефектов
|
3
|
0
|
Герметизация кожных швов
|
5
|
1 (воспалительная реакция)
|
Профилактика лимфокист при операциях на органах малого таза
|
2
|
1 (температурная реакция)
|
ИТОГО:
|
33
|
4 (13,3%)
|
Таблица 4. Применение клея латексного тканевого (ЛТК) при операциях на гортани
Категория пациентов
|
Количество
|
Первичное заживление
|
Послеоперационные осложнения(свищи глотки)
|
Первичные больные
|
4
|
4
|
-
|
После полной дозы лучевой терапии
|
5
|
5
|
-
|
После предоперационного курса лучевой терапии
|
3
|
2
|
1
|
После химиотерапии
|
2
|
2
|
-
|
ИТОГО
с использованием клея
|
14
|
13
|
1 (7,14%)
|
Контрольная группа без использования клея
|
11
|
8
|
3 (27,7%)
|
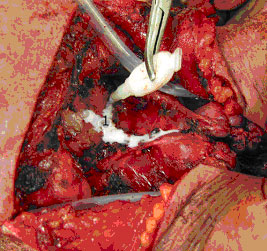
Рисунок 1. Методика нанесения клея на линию глоточного шва после ларингэктомии
 |
 |
1-клеем обрабатывается весь длинник глоточного шва
|
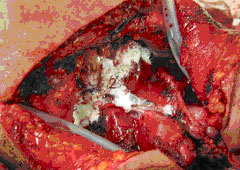
2 – вид операционной раны после нанесения клея на глотку
|
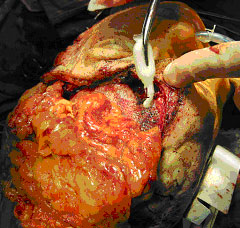
Рисунок 2. Методика использования клея при дефектах ТМО
 |
 |
1 - Клеем дополнительно герметизируется дефект ТМО, после пластики полипропиленовой сеткой
|
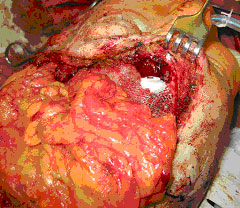
2 – Вид операционной раны после нанесения клея на полипропиленовую сетку, в зону дефекта ТМО
|
Рисунок 3. Использование клея при пластике сосудов
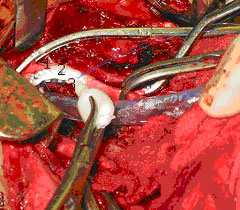 |
1 - плечеголовной ствол справа
2 – сосудистый протез
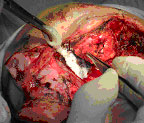
Рисунок 4. Пример использования клея для герметизации клеток решётчатого лабиринта
 |
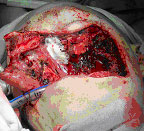 |
1 – клеем обрабатываются передние клетки решетчатого лабиринта
2 – параорбитальная клетчатка
|
3 - вид операционной раны после нанесения клея
|
Используемая литература:
3. Попов В.А., Сиротинкин Н.В., Головаченко В.А. Латексный тканевый клей и его применение в хирургии. // Научно-практический журнал «Полимеры и Медицина». – СПб, 2(1)/2006, стр. 25–26.
4. Плужников М.С., М.А.Рябова, Н.А.Шумилова. Применение латексного тканевого клея в отоларингологии. // Folia Otorhinolaringologiae et Pathologiae Respiratoriae, v. 12, № 1-2, СПб, 2006, стр. 73-78.
5. Попов В.А., Пышков Е.А. Разработка нового латексного тканевого клея и пути повышения его биосовместимости // Тезисы докл. конф. II факультета. - СПб., ВМедА, 2002. - С.63.
6. Попов В.А., Пышков Е.А. Способ нанесения на зону кишечного анастомоза и раны паренхиматозных органов латексного тканевого клея // Сборник изобретений и рационализаторских предложений. Усовершенствование методов и аппаратуры, применяемых в учебном процессе, медико-биологических исследованиях и клинической практике. - СПб., ВМедА, 2003 - № 34. – С.58–59.
7. Пучков К. В., Селиверстов Д. В., Полит Г. Г., Гаусман Б. Я. Новые синтетические материалы в хирургии /К. В. Пучков, Д. В. Селиверстов, Г. Г. Полит, Б. Я. Гаусман. - Рязань, 1994. – 44 с.
8. Бокерия Л.А., Муратов Р.М., Межнева В.В., Костава В.Т., Крестинич И.М., Абасов М.М. Клиническое применение нового биологического клея «Биоклей-ЛАБ» при операциях на сердце в условиях искусственного кровообращения. //Хирургия. Журнал им. Н.И.Пирогова – 2005.-№1.-с.18-20.
9. Попов В.А., Пышков Е.А. Способ определения глубины диффузии гидрофильных тканевых клеев в биологической ткани // Тезисы докл. конф. II факультета. - СПб., ВМедА, 2002.- С.63.
10. Марченко В.Т., Прутовых Н.Н., Толстиков Г.А., Толстиков А.Г. Медицинский клей «Сульфакрилат». Антибактериальная противовоспалительная клеевая композиция.// Руководство для применения в хирургических областях. 2005.-с.-80.
11. А.Г. Толстиков, Г.А. Толстиков, А.И. Воробьева, А.А. Лобанова, Б.В. Ларионов. Отечественный медицинский клей «Сульфакрилат».
12. McCarthy PM. Fibrin glue in cardiothoracic surgery. Transfus Med Rev. 1993;7(3):173–179 July
13. Douglas M. Sidle, MD; Benjamin M. Loos, MD; Alexander L. Ramirez, MD; Sheldon S. Kabaker, MD; Corey S. Maas, MD Use of BioGlue Surgical Adhesive for Brow Fixation in Endoscopic Browplasty. Arch Facial Plast Surg. 2005;7:393-397
14. Efficacy and Safety of Endotine Fixation Device in Endoscopic Brow-Lift Byrne Arch Facial Plast Surg 2007;9:212-214.
15. L. Lang-Lazdunski Closure of a bronchopleural fistula after extended right pneumonectomy after induction chemotherapy with BioGlue surgical adhesive J. Thorac. Cardiovasc. Surg., December 1, 2006; 132(6): 1497–1498
16. A. Malik, M. Oc, G. Doukas, C. Alexiou, and T. J Spyt Early Failure of Surgical Angioplasty with Tissue Glue: a Word of Caution Asian Cardiovasc Thorac Ann, October 1, 2006; 14(5): e91–e92.
17. P. Tansley, F. Al-Mulhim, E. Lim, G. Ladas, and P. Goldstraw A prospective, randomized, controlled trial of the effectiveness of BioGlue in treating alveolar air leaks J. Thorac. Cardiovasc. Surg., July 1, 2006; 132(1): 105–112
18. A. Szafranek, S.R. Podila, W. Al-Khyatt, and E.N. Kulatilake Aseptic mediastinal cyst caused by BioGlue 7 months after cardiac surgery J. Thorac. Cardiovasc. Surg., May 1, 2006; 131(5): 1202 – 1203.
19. D. M. Sidle, B. M. Loos, A. L. Ramirez, S. S. Kabaker, and C. S. Maas Use of BioGlue Surgical Adhesive for Brow Fixation in Endoscopic Browplasty Arch Facial Plast Surg, November 1, 2005; 7(6): 393 - 397.
20. Y. Van Belleghem, R. G. Forsyth, K. Narine, A. Moerman, Y. Taeymans, and G. J. Van Nooten Bovine glue (BioGlue) is catabolized by enzymatic reaction in the vascular dog model Ann. Thorac. Surg., June 1, 2004; 77(6): 2177 - 2181.
21. Jeffrey N. Bloom, MD; Mark T. Duffy, MD, PhD; Jason B. Davis, BS; Karen M. McNally-Heintzelman, PhD A Light-Activated Surgical Adhesive Technique for Sutureless Ophthalmic Surgery Arch Ophthalmol. 2003;121:1591-1595.
|


